ما الذي يحتوي على طاقة كامنة أكبر الماء أم الجلوكوز
تتجاوز الطاقة الكيميائية الكامنة التي تخزنها جزيئات الجلوكوز (C≡H≡O₂) بشكل كبير مستوى جزيء ماء واحد (H₂O). يمكن أن يُعزى هذا الاختلاف الكبير إلى 3 عوامل أساسية على المستوى الجزيئي: الأول هو الاختلاف الكبير في التعقيد الجزيئي وعدد الروابط الكيميائية، والثاني هو نوع الروابط الكيميائية وثباتها، وأخيرًا حالة أكسدة ذرة الكربون. هذه العوامل هي التي تحدد أن الجلوكوز هو مصدر الطاقة الرئيسي للحياة، والماء هو الوسط المستقر للتفاعل الكيميائي للحياة.
التعقيد الجزيئي وعدد الروابط الكيميائية
أولًا، لنلقِ نظرة على التركيب الجزيئي. يتكون جزيء الجلوكوز من 24 ذرة متصلة ب 24 رابطة تساهمية، وبنيته معقدة للغاية. وعلى النقيض من ذلك، يتكون جزيء الماء من ثلاث ذرات فقط وروابط تساهمية. لنكون صادقين، هذه ليست مقارنة من حيث الحجم على الإطلاق في التركيب. تُخزَّن طاقة الجزيء في روابطه الكيميائية، لذا فإن الروابط الكيميائية الأكثر في الجلوكوز تسمح له بتخزين طاقة كامنة أكثر بكثير من الماء. وعندما تنكسر هذه الروابط الكيميائية أثناء عمليات مثل التنفس الخلوي، تتحرر الطاقة المخزنة لتستخدمها الخلية.
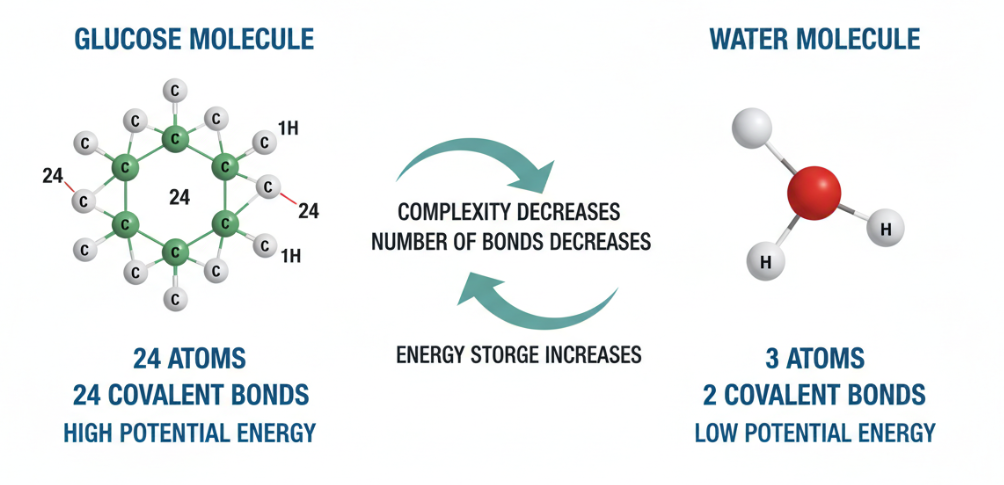
نوع الرابطة الكيميائية وثباتها
العامل التالي، هو مفتاح فهم فرق الطاقة: نوع الرابطة الكيميائية واستقرارها. يحتوي الجلوكوز على عدد كبير من الروابط بين الكربون والكربون (C-C) والكربون والهيدروجين (C-H). وبالمقارنة مع روابط الأكسجين والهيدروجين (O-H) المستقرة للغاية في الماء، فإن روابط C-C و C-H هذه غير مستقرة نسبيًا وبالتالي تحتوي على طاقة أعلى. ويرجع السبب في أن حالة طاقة رابطة O-H في الماء أقل إلى أن ذرة الأكسجين لها سالبية كهربية قوية، مما يجعل إلكترونات الرابطة أكثر انحيازًا نحو الأكسجين، وبالتالي تشكل بنية مستقرة للغاية. وهذا ما يفسر سبب كون التنفس الخلوي عملية إطلاق للطاقة. في هذه العملية، يتكسر الجلوكوز في وجود الأكسجين إلى ثاني أكسيد الكربون والماء، وكلاهما جزيئات أقل طاقة وأكثر استقرارًا. والطاقة المنطلقة من هذه العملية هي في الأساس نتيجة لانتقال الإلكترونات من حالات الطاقة العالية لذرات الكربون والهيدروجين الأقل كهربة في الجلوكوز إلى ذرات الأكسجين الأكثر كهربة لتكوين حالة أقل طاقة وأكثر استقرارًا.
إلى طليعة التغذية
نقدم دائمًا معايير عالية من المضافات الغذائية والتغذية، ونقدم حلولاً مبتكرة تعزز النكهة والقوام والمظهر الغذائي للأغذية، وتدعم المنتجات الصحية والمستدامة لصناعة الأغذية.
حالة تأكسد الكربون
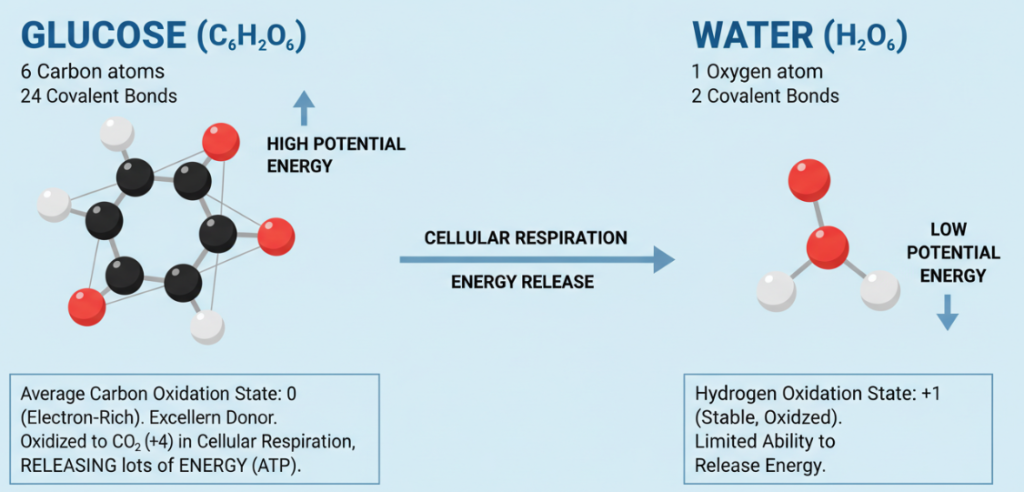
أخيرًا، يجب أن نتحدث عن حالة تأكسد ذرة الكربون، ويمكن القول إن هذا مؤشر حاسم على الطاقة الكامنة العالية للجلوكوز. في الجلوكوز، تكون ذرات الكربون في حالة مختزلة للغاية، ما يعني أنها غنية بالإلكترونات. بعد الحساب، يكون متوسط حالة أكسدة ذرات الكربون في الجلوكوز 0. هذا الفائض من الإلكترونات يجعل الجلوكوز مانحًا ممتازًا للإلكترونات. أثناء التنفس الخلوي، تتأكسد ذرات الكربون في الجلوكوز لتكوين ثاني أكسيد الكربون (CO₂). في ثاني أكسيد الكربون، تتغير حالة أكسدة ذرة الكربون إلى +4، ما يشير إلى أنها فقدت إلكترونًا. وتنتقل الإلكترونات نحو ذرات الأكسجين الأكثر كهربةً، فتطلق الكثير من الطاقة التي يتم التقاطها بعد ذلك في شكل أدينوسين ثلاثي الفوسفات الأحادي (3 أدينوزين أحادي الفوسفات) لتشغيل نشاط الخلية. ومن ناحية أخرى، تكون ذرات الهيدروجين في جزيئات الماء في حالة مستقرة ومؤكسدة بالفعل، وتكون قدرتها على إطلاق المزيد من الطاقة محدودة للغاية.
المؤلف: بيل
بصفتي متخصصًا شغوفًا ومهتمًا بعمق في الكيمياء الحيوية، فقد قضيت سنوات في تحليل المفاهيم العلمية المعقدة إلى محتوى واضح وسهل الوصول إليه. في هذه المقالة، أتعمق في الفروق الجزيئية التي تجعل الجلوكوز مصدرًا للطاقة الكامنة مقارنةً بالماء. آمل أن ألقي الضوء على المبادئ الأساسية التي تحكم الطاقة في الأنظمة البيولوجية، مما يساعد القراء على فهم السبب الذي يجعل هذين الجزيئين البسيطين في الظاهر يلعبان دورًا مختلفًا إلى حد كبير في الحفاظ على الحياة.
 SGNUTRI
SGNUTRI