لماذا يذوب الجلوكوز في الماء؟
والسبب الأساسي وراء ذوبان الجلوكوز في الماء هو أن كلاهما "جزيئات قطبية"، وهو ما يسمح لجزيئات الماء بتكوين تجاذبات قوية تسمى "روابط هيدروجينية" مع جزيئات الجلوكوز. وعلى وجه التحديد، يحتوي جزيء الجلوكوز على مجموعات هيدروكسيل (-OH) قطبية متعددة. كما أن جزيء الماء (H₂O↩O) قطبي أيضًا، حيث تكون ذرة الأكسجين فيه سالبة قليلًا وذرات الهيدروجين فيه موجبة قليلًا. عندما يدخل الجلوكوز في الماء، تنجذب جزيئات الماء، التي تعمل مثل مغناطيسات صغيرة، إلى مجموعات الهيدروكسيل الموجودة على جزيء الجلوكوز وتشكل روابط هيدروجينية معها. هذا التجاذب قوي بما يكفي للتغلب على القوى التي تمسك جزيئات الجلوكوز معًا في شكلها البلوري الصلب. ونتيجة لذلك، "تُسحب" جزيئات الجلوكوز المنفردة من البلورة وتصبح مشتتة بالتساوي بين جزيئات الماء، وهي عملية نلاحظ أنها عملية ذوبان.
قطبية الجزيئات
في الكيمياء، يعد مبدأ "الشبيه يذوب الشبيه" أساسيًا ويفسر تمامًا العلاقة بين الجلوكوز والماء. فكلاهما ينتمي إلى الجزيئات القطبية، وهذه الأرضية المشتركة هي التي تحدد إمكانية "قبول" كل منهما للآخر. وبعبارة صريحة، قطبية الجزيء هي ما إذا كان توزيع شحنته الداخلية منتظمًا. وهذا بدوره ينبع من الاختلافات في "السالبية الكهربية"، أي قدرة الذرات على جذب الإلكترونات المشتركة في الروابط الكيميائية.
الماء (H₂O): في جزيء الماء، تكون ذرتا الأكسجين أكثر سالبية كهربية من ذرتي الهيدروجين. هذا يعني أن إلكترونات الترابط ستكون أكثر انحيازًا نحو ذرة الأكسجين، مما يعطيها شحنة سالبة ضعيفة (δ-)، بينما ذرتا الهيدروجين ستُترك لهما شحنة موجبة ضعيفة (δ+). هذا الفصل بين الشحنات، إلى جانب حقيقة أن جزيء الماء نفسه عبارة عن بنية "منحنية" على شكل حرف V، يجعله جزيئًا قطبيًا نموذجيًا للغاية مع نهايات موجبة وسالبة واضحة.

الغلوكوز (C₆H₁₂O₆): على الرغم من أن جزيء الجلوكوز أكبر بكثير، إلا أن المبدأ هو نفسه. فهو يحتوي على العديد من مجموعات الهيدروكسيل (-OH) في بنيته. وفي كل مجموعة هيدروكسيل يكون الأكسجين أكثر سالبية كهربية من الهيدروجين والكربون المرتبطين به. وينتج عن ذلك فصل كبير للشحنة داخل كل مجموعة -OH، مما يجعلها قطبية للغاية. ومع وجود هذا العدد الكبير من المجموعات شديدة القطبية في الجزيء، يصبح جزيء الجلوكوز بأكمله جزيئًا قطبيًا بطبيعة الحال.
الروابط الهيدروجينية
ونظرًا لأن الجلوكوز والماء قطبيان، فإنهما يهيئان الظروف الملائمة لتكوين قوة بين جزيئية قوية - الرابطة الهيدروجينية. الرابطة الهيدروجينية هي تجاذب خاص وقوي إلى حد ما. وهي تحدث عادةً بين ذرة هيدروجين مرتبطة بذرة ذات سالبية كهربية قوية (مثل الأكسجين أو النيتروجين أو الفلور) وذرة أخرى قريبة ذات سالبية كهربية.
عندما يوضع الجلوكوز الصلب في الماء، يكون لجزيئات الماء طرف هيدروجين ضعيف الشحنة موجب الشحنة وتنجذب بقوة إلى ذرات الأكسجين الضعيفة سالبة الشحنة في مجموعة هيدروكسيل الجلوكوز. وعلى العكس، ينجذب طرف الأكسجين الضعيف سالب الشحنة في جزيء الماء أيضًا إلى ذرات الهيدروجين الضعيفة الشحنة الموجبة الشحنة في مجموعة هيدروكسيل الجلوكوز. هذه الشبكة الجاذبة بين هذين الجزيئين هي جوهر الرابطة الهيدروجينية في هذا السيناريو.
إلى طليعة التغذية
نقدم دائمًا معايير عالية من المضافات الغذائية والتغذية، ونقدم حلولاً مبتكرة تعزز النكهة والقوام والمظهر الغذائي للأغذية، وتدعم المنتجات الصحية والمستدامة لصناعة الأغذية.
عملية الحل
إن انحلال الجلوكوز هو عملية لعبة ديناميكية على المستوى الجزيئي.
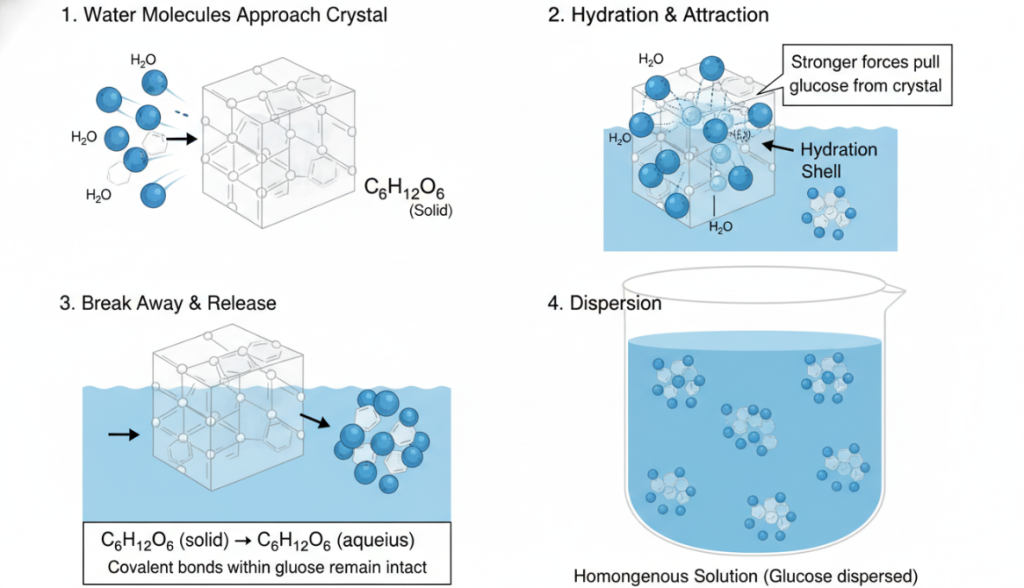
تقترب جزيئات الماء من البلورات: في الحالة الصلبة، يوجد الجلوكوز في شكل شبكة بلورية، وترتبط الجزيئات المنفردة ببعضها البعض بواسطة القوى بين الجزيئية الخاصة بها. عندما تُلقى هذه البلورة في الماء، تبدأ جزيئات الماء المتحركة في الاصطدام بسطحها.
الترطيب والجذب: تحيط جزيئات الماء القطبية مباشرة بجزيئات الجلوكوز على سطح البلورة. من خلال تكوين عدد كبير من الروابط الهيدروجينية، تصبح قوة جذب مجموعة من جزيئات الماء إلى جزيء جلوكوز واحد أقوى من القوة بين جزيء الجلوكوز هذا وجيرانه في البلورة.
ينفصل ويتحرر: يسحب هذا "السحب" القوي من جزيئات الماء جزيئات الجلوكوز المنفردة من البنية الصلبة. ويجب التأكيد هنا على أن جزيء الماء لا يكسر الروابط التساهمية القوية داخل جزيء الجلوكوز؛ بل يكسر فقط القوى الأضعف بين الجزيئات التي تحافظ على البنية البلورية. والنتيجة هي أن جزيئات الجلوكوز السليمة تنفصل عن البلورة وتنتقل إلى المحلول. يُعبَّر عن هذه العملية عادةً بهذه المعادلة C₆H₁₁₂O₆ (صلب) → C₆H₁₁₂₂O₆ (مائي).
المؤلفديريك
يكمن شغفي في إزالة الغموض عن الكيمياء. أحب أن أطرح سؤالاً بسيطاً، مثل "لماذا يذوب السكر في الماء؟"، وأحب أن أكشف عن العلم الجزيئي الأنيق وراء ذلك، مع التركيز على الأفكار الأساسية مثل القطبية وقوة الرابطة الهيدروجينية.
 SGNUTRI
SGNUTRI