¿Por qué la glucosa es soluble en agua?
La razón principal por la que la glucosa se disuelve en agua es que ambas son "moléculas polares", lo que permite a las moléculas de agua formar fuertes atracciones llamadas "enlaces de hidrógeno" con las moléculas de glucosa. En concreto, una molécula de glucosa tiene múltiples grupos hidroxilo (-OH) polares. La molécula de agua (H₂O) también es polar, con su átomo de oxígeno ligeramente negativo y sus átomos de hidrógeno ligeramente positivos. Cuando la glucosa entra en el agua, las moléculas de agua, que actúan como pequeños imanes, se sienten atraídas por los grupos hidroxilo de la molécula de glucosa y forman enlaces de hidrógeno con ellos. Esta atracción es lo suficientemente poderosa como para superar las fuerzas que mantienen unidas a las moléculas de glucosa en su forma de cristal sólido. En consecuencia, las moléculas individuales de glucosa son "arrancadas" del cristal y se dispersan uniformemente entre las moléculas de agua, un proceso que observamos como disolución.
Polaridad de las moléculas
En química, el principio de "lo semejante se disuelve en lo semejante" es fundamental y explica perfectamente la relación entre la glucosa y el agua. Ambas pertenecen a las moléculas polares, y es este punto en común el que determina que puedan "aceptarse" mutuamente. La polaridad de una molécula, por decirlo sin rodeos, es si su distribución interna de cargas es uniforme. Esto, a su vez, se deriva de las diferencias en la "electronegatividad", es decir, la capacidad de los átomos para atraer electrones compartidos en los enlaces químicos.
Agua (H₂O): En una molécula de agua, los átomos de oxígeno son mucho más electronegativos que los dos átomos de hidrógeno. Esto significa que los electrones de enlace estarán más sesgados hacia el átomo de oxígeno, dándole una débil carga negativa (δ-), mientras que los dos átomos de hidrógeno se quedarán con una débil carga positiva (δ+). Esta separación de cargas, unida al hecho de que la propia molécula de agua es una estructura "curva" en forma de V, la convierte en una molécula polar muy típica con extremos positivos y negativos claros.

Glucosa (C₆H₁₂O₆): Aunque la molécula de glucosa es mucho más grande, el principio es el mismo. Tiene muchos grupos hidroxilo (-OH) en su estructura. En cada grupo hidroxilo, el oxígeno es más electronegativo que el hidrógeno y el carbono unidos a él. El resultado es una separación significativa de la carga dentro de cada grupo -OH, lo que lo hace muy polar. Con tantos grupos altamente polares en una molécula, toda la molécula de glucosa se convierte naturalmente en una molécula polar.
Enlaces de hidrógeno
Precisamente porque la glucosa y el agua son polares, se crean las condiciones para la formación de una fuerte fuerza intermolecular: el enlace de hidrógeno. Un enlace de hidrógeno es una atracción especial y bastante fuerte. Suele producirse entre un átomo de hidrógeno que se ha unido a un átomo fuertemente electronegativo (como el oxígeno, el nitrógeno o el flúor) y otro átomo electronegativo cercano.
Cuando la glucosa sólida se coloca en agua, las moléculas de agua tienen un extremo de hidrógeno débilmente cargado positivamente y son fuertemente atraídas por los átomos de oxígeno débilmente cargados negativamente en el grupo hidroxilo de la glucosa. A la inversa, el extremo de oxígeno débilmente cargado negativamente de la molécula de agua también es atraído por los átomos de hidrógeno débilmente cargados positivamente del grupo hidroxilo de la glucosa. Esta red de atracción entre estas dos moléculas es la esencia del enlace de hidrógeno en este escenario.
A la vanguardia de la nutrición
Proporcionamos soluciones innovadoras que mejoran el sabor, la textura y el perfil nutricional de los alimentos, apoyando productos más saludables y sostenibles para la industria alimentaria.
Proceso de disolución
La disolución de la glucosa es un proceso de juego dinámico a nivel molecular.
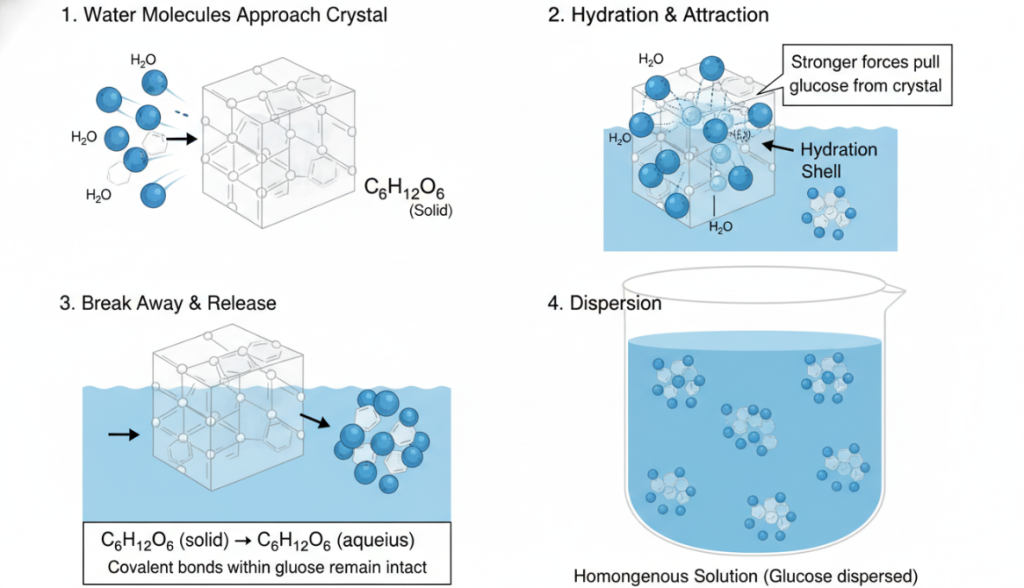
Las moléculas de agua se acercan a los cristales: En estado sólido, la glucosa existe en forma de red cristalina, y las moléculas individuales se mantienen unidas entre sí por sus propias fuerzas intermoleculares. Cuando este cristal se lanza al agua, las moléculas de agua en movimiento empiezan a chocar contra su superficie.
Hidratación y atracción: Las moléculas polares de agua rodean inmediatamente a las moléculas de glucosa en la superficie del cristal. Al formar un gran número de enlaces de hidrógeno, la atracción de un grupo de moléculas de agua hacia una sola molécula de glucosa se hace más fuerte que la fuerza entre esa molécula de glucosa y sus vecinas en el cristal.
Desprenderse y liberarse: Este potente "tirón" de las moléculas de agua arranca eficazmente moléculas individuales de glucosa de la estructura sólida. Hay que destacar aquí que la molécula de agua no rompe los fuertes enlaces covalentes dentro de la molécula de glucosa; sólo rompe las fuerzas intermoleculares más débiles que mantienen la estructura cristalina. El resultado es que las moléculas de glucosa intactas se desprenden del cristal y pasan a la solución. Este proceso suele expresarse mediante esta ecuación: C₆H₁₂O₆ (sólido) → C₆H₁₂O₆ (acuoso).
Autor:Derek
Mi pasión es desmitificar la química. Me encanta plantear una pregunta sencilla, como "¿por qué se disuelve el azúcar en el agua?", y revelar la elegante ciencia molecular que hay detrás, centrándome en ideas fundamentales como la polaridad y el poder del enlace de hidrógeno.
 SGNUTRI
SGNUTRI