Warum ist Glukose in Wasser löslich?
Der Hauptgrund dafür, dass sich Glukose in Wasser auflöst, ist, dass es sich bei beiden um "polare Moleküle" handelt, die es den Wassermolekülen ermöglichen, mit den Glukosemolekülen starke Anziehungskräfte, sogenannte "Wasserstoffbrücken", zu bilden. Ein Glukosemolekül hat nämlich mehrere polare Hydroxylgruppen (-OH). Das Wassermolekül (H₂O) ist ebenfalls polar, wobei sein Sauerstoffatom leicht negativ und seine Wasserstoffatome leicht positiv sind. Wenn Glukose in Wasser eintritt, werden die Wassermoleküle wie winzige Magnete von den Hydroxylgruppen des Glukosemoleküls angezogen und bilden mit ihnen Wasserstoffbrückenbindungen. Diese Anziehungskraft ist stark genug, um die Kräfte zu überwinden, die die Glukosemoleküle in ihrer festen Kristallform zusammenhalten. Infolgedessen werden einzelne Glukosemoleküle aus dem Kristall "herausgezogen" und gleichmäßig unter den Wassermolekülen verteilt, ein Vorgang, den wir als Auflösen beobachten.
Polarität von Molekülen
In der Chemie ist das Prinzip "Gleiches löst Gleiches" grundlegend und erklärt perfekt die Beziehung zwischen Glukose und Wasser. Beide gehören zu den polaren Molekülen, und es ist diese Gemeinsamkeit, die bestimmt, dass sie sich gegenseitig "akzeptieren" können. Die Polarität eines Moleküls ist, vereinfacht ausgedrückt, die Gleichmäßigkeit seiner inneren Ladungsverteilung. Diese wiederum ergibt sich aus Unterschieden in der "Elektronegativität" - der Fähigkeit der Atome, in chemischen Bindungen gemeinsame Elektronen anzuziehen.
Wasser (H₂O): In einem Wassermolekül sind die Sauerstoffatome viel elektronegativer als die beiden Wasserstoffatome. Das bedeutet, dass die Bindungselektronen stärker auf das Sauerstoffatom gerichtet sind und ihm eine schwache negative Ladung (δ-) verleihen, während die beiden Wasserstoffatome mit einer schwachen positiven Ladung (δ+) zurückbleiben. Diese Ladungstrennung in Verbindung mit der Tatsache, dass das Wassermolekül selbst eine V-förmig "gekrümmte" Struktur aufweist, macht es zu einem sehr typischen polaren Molekül mit klaren positiven und negativen Enden.

Glukose (C₆H₁₂O₆): Obwohl das Glukosemolekül viel größer ist, ist das Prinzip das gleiche. Es hat viele Hydroxylgruppen (-OH) in seiner Struktur. In jeder Hydroxylgruppe ist der Sauerstoff elektronegativer als der daran gebundene Wasserstoff und Kohlenstoff. Dies führt zu einer erheblichen Ladungstrennung innerhalb jeder -OH-Gruppe und macht sie sehr polar. Mit so vielen hochpolaren Gruppen in einem Molekül wird das gesamte Glukosemolekül natürlich zu einem polaren Molekül.
Wasserstoff-Bindungen
Gerade weil Glukose und Wasser polar sind, schaffen sie die Voraussetzungen für die Bildung einer starken zwischenmolekularen Kraft, der Wasserstoffbindung. Eine Wasserstoffbrückenbindung ist eine besondere, ziemlich starke Anziehungskraft. Sie entsteht in der Regel zwischen einem Wasserstoffatom, das an ein stark elektronegatives Atom (wie Sauerstoff, Stickstoff oder Fluor) gebunden ist, und einem anderen elektronegativen Atom in der Nähe.
Wenn feste Glukose in Wasser gegeben wird, haben die Wassermoleküle ein schwach positiv geladenes Wasserstoffende und werden stark von den schwach negativ geladenen Sauerstoffatomen in der Hydroxylgruppe der Glukose angezogen. Umgekehrt wird das schwach negativ geladene Sauerstoffende des Wassermoleküls auch von den schwach positiv geladenen Wasserstoffatomen in der Glukosehydroxylgruppe angezogen. Dieses anziehende Netzwerk zwischen diesen beiden Molekülen ist das Wesen der Wasserstoffbrückenbindung in diesem Szenario.
An der Spitze der Ernährung
Wir bieten innovative Lösungen, die den Geschmack, die Beschaffenheit und das Nährwertprofil von Lebensmitteln verbessern, und unterstützen gesündere, nachhaltige Produkte für die Lebensmittelindustrie.
Auflösungsprozess
Die Auflösung von Glukose ist ein dynamischer Spielprozess auf molekularer Ebene.
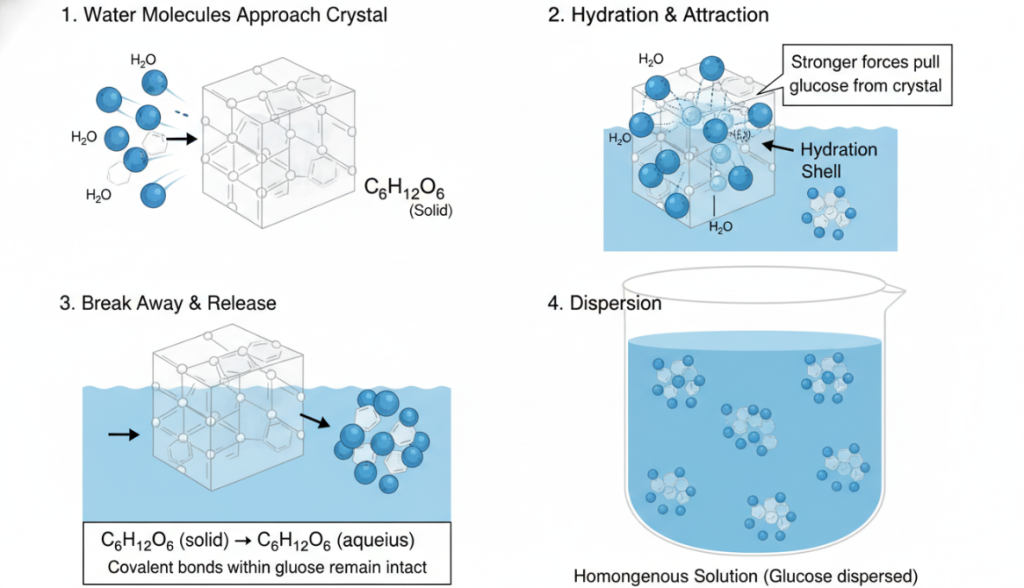
Wassermoleküle nähern sich den Kristallen: Im festen Zustand liegt Glukose in Form eines Kristallgitters vor, und die einzelnen Moleküle werden durch ihre eigenen intermolekularen Kräfte aneinander gehalten. Wenn dieser Kristall ins Wasser geworfen wird, beginnen die sich bewegenden Wassermoleküle auf seine Oberfläche zu treffen.
Hydratation und Anziehung: Polare Wassermoleküle umgeben die Glukosemoleküle auf der Oberfläche des Kristalls unmittelbar. Durch die Bildung einer großen Anzahl von Wasserstoffbrückenbindungen wird die Anziehungskraft einer Gruppe von Wassermolekülen auf ein einzelnes Glukosemolekül stärker als die Kraft zwischen diesem Glukosemolekül und seinen Nachbarn im Kristall.
Wegbrechen und Freisetzen: Diese starke "Anziehungskraft" der Wassermoleküle zieht einzelne Glukosemoleküle effektiv aus der festen Struktur heraus. Es muss hier betont werden, dass das Wassermolekül nicht die starken kovalenten Bindungen innerhalb des Glukosemoleküls aufbricht; es bricht nur die schwächeren zwischenmolekularen Kräfte, die die Kristallstruktur aufrechterhalten. Das Ergebnis ist, dass intakte Glukosemoleküle aus dem Kristall ausbrechen und in Lösung gehen. Dieser Prozess wird in der Regel durch diese Gleichung ausgedrückt: C₆H₁₂O₆ (fest) → C₆H₁₂O₆ (wässrig).
Autor"Derek
Meine Leidenschaft gilt der Entmystifizierung der Chemie. Ich liebe es, eine einfache Frage wie "Warum löst sich Zucker in Wasser auf?" aufzugreifen und die elegante molekulare Wissenschaft dahinter zu enthüllen, wobei ich mich auf Kernideen wie Polarität und die Kraft der Wasserstoffbindung konzentriere.
 SGNUTRI
SGNUTRI