グルコースはなぜ水に溶けるのか
グルコースが水に溶ける主な理由は、両者が「極性分子」であるため、水分子がグルコース分子と「水素結合」と呼ばれる強い引力を形成するためである。具体的には、グルコース分子は複数の極性水酸基(-OH)を持っている。水分子(H₂O)も極性を持ち、酸素原子はわずかに負、水素原子はわずかに正である。グルコースが水に入ると、水分子は小さな磁石のように働き、グルコース分子の水酸基に引き寄せられ、水素結合を形成する。この引力は、固体の結晶状態でグルコース分子同士を結びつけている力に打ち勝つほど強力である。その結果、個々のグルコース分子は結晶から「引き離され」、水分子中に均一に分散するようになる。
分子の極性
化学では、「類は友を呼ぶ」という原則が基本であり、グルコースと水の関係を完璧に説明している。両者とも極性分子に属し、この共通項がお互いを「受け入れる」ことを決定している。分子の極性とは、単刀直入に言えば、分子の内部の電荷分布が均一かどうかということである。これは、「電気陰性度」(化学結合において共有電子を引き寄せる原子の能力)の違いに由来する。
水(H₂O):水分子において、酸素原子は2つの水素原子よりもはるかに電気陰性である。つまり、結合電子は酸素原子に偏って弱い負電荷(δ-)を帯び、2つの水素原子は弱い正電荷(δ+)を帯びる。この電荷の分離は、水分子自体がV字型の "曲がった "構造であることと相まって、プラスとマイナスの両端がはっきりした非常に典型的な極性分子となっている。

グルコース(C₆H₁₂O₆):グルコース分子ははるかに大きいが、原理は同じである。グルコースの構造には多くの水酸基(-OH)がある。それぞれの水酸基において、酸素はそれに結合している水素や炭素よりも電気陰性度が高い。その結果、それぞれの-OH基の中で電荷が大きく分離し、非常に極性の高い基となる。分子上に非常に多くの極性基を持つため、グルコース分子全体が自然に極性分子になる。
水素結合
グルコースと水が極性であるからこそ、強い分子間力-水素結合-を形成する条件が整うのである。水素結合は特殊で、かなり強い引力である。水素結合は通常、電気陰性度の強い原子(酸素、窒素、フッ素など)と結合した水素原子と、その近くにある別の電気陰性度の高い原子との間に生じる。
固体のグルコースを水に入れると、水分子は弱くプラスに帯電した水素末端を持ち、グルコース水酸基の弱くマイナスに帯電した酸素原子に強く引き寄せられる。逆に、水分子の弱く負に帯電した酸素末端も、グルコース水酸基の弱く正に帯電した水素原子に引き寄せられる。この2つの分子間の引き合うネットワークが、このシナリオにおける水素結合の本質である。
解散プロセス
グルコースの溶解は、分子レベルでのダイナミックなゲームプロセスである。
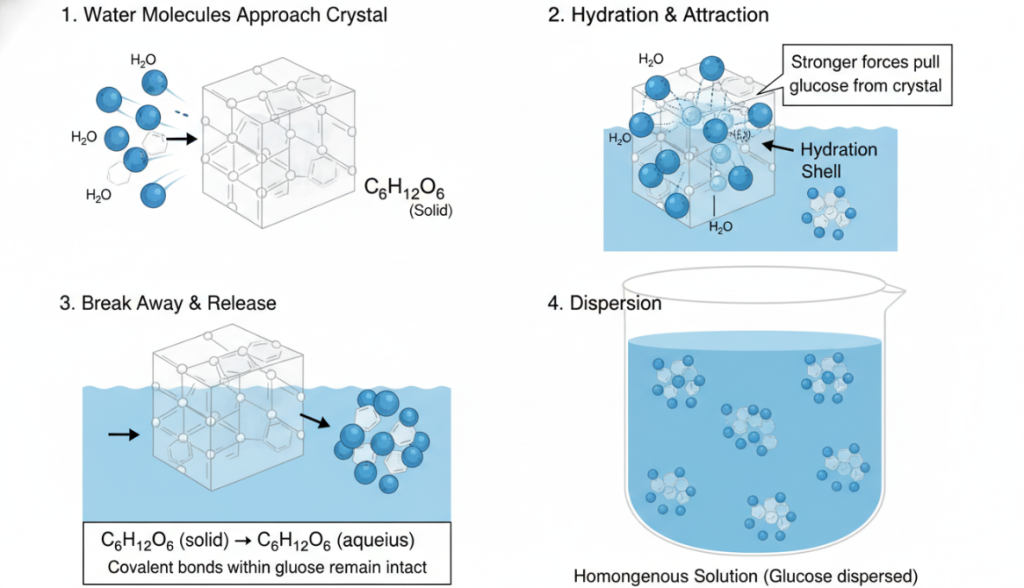
水分子が結晶に近づく:固体状態では、グルコースは結晶格子の形で存在し、個々の分子はそれぞれの分子間力によって互いに保持されている。この結晶を水中に投げ入れると、動いている水分子がその表面にぶつかり始める。
水和と引力:結晶表面のグルコース分子を極性の高い水分子がすぐに取り囲む。多数の水素結合を形成することで、グルコース分子1つに対する水分子グループの引力は、結晶中のグルコース分子とその隣の分子との間の力よりも強くなる。
離脱と放出:水分子によるこの強力な「引力」は、個々のグルコース分子を固体構造から効果的に引き離す。ここで強調しなければならないのは、水分子はグルコース分子内の強い共有結合を切断するのではなく、結晶構造を維持する弱い分子間力を切断するだけだということである。その結果、無傷のグルコース分子が結晶から抜け出し、溶液になる。この過程は通常、次の式で表される:C₆H₂₁O₂ (固体) → C₆H₂O₆ (水溶液)。
著者デレク
私の情熱は化学を解明することにある。なぜ砂糖は水に溶けるのか」というような素朴な疑問を取り上げ、極性や水素結合の力といった核となる考え方に焦点を当てながら、その背後にあるエレガントな分子科学を明らかにするのが好きだ。
 SGNUTRI
SGNUTRI