Was hat mehr potenzielle Energie - Wasser oder Glukose?
Die von Glukosemolekülen (C≡H≡O₂) gespeicherte chemische potenzielle Energie übersteigt die eines Wassermoleküls (H₂O) erheblich. Dieser signifikante Unterschied lässt sich auf drei zentrale Faktoren auf molekularer Ebene zurückführen: zum einen auf den großen Unterschied in der molekularen Komplexität und der Anzahl der chemischen Bindungen, zum anderen auf die Art und Stabilität der chemischen Bindungen und schließlich auf den Oxidationszustand des Kohlenstoffatoms. Diese Faktoren sind ausschlaggebend dafür, dass Glukose die Hauptenergiequelle des Lebens und Wasser das stabile Medium der chemischen Reaktion des Lebens ist.
Molekulare Komplexität und die Anzahl der chemischen Bindungen
Schauen wir uns zunächst die Molekularstruktur an. Ein Glukosemolekül besteht aus 24 Atomen, die durch 24 kovalente Bindungen verbunden sind, und die Struktur ist recht komplex. Im Gegensatz dazu besteht ein Wassermolekül aus nur drei Atomen und zwei kovalenten Bindungen. Um ehrlich zu sein, handelt es sich hier nicht um einen Größenvergleich in der Struktur. Die Energie eines Moleküls wird in seinen chemischen Bindungen gespeichert, so dass Glukose aufgrund der größeren Anzahl chemischer Bindungen viel mehr potenzielle Energie speichern kann als Wasser. Wenn diese chemischen Bindungen bei Prozessen wie der Zellatmung aufgebrochen werden, wird die gespeicherte Energie zur Nutzung durch die Zelle freigegeben.
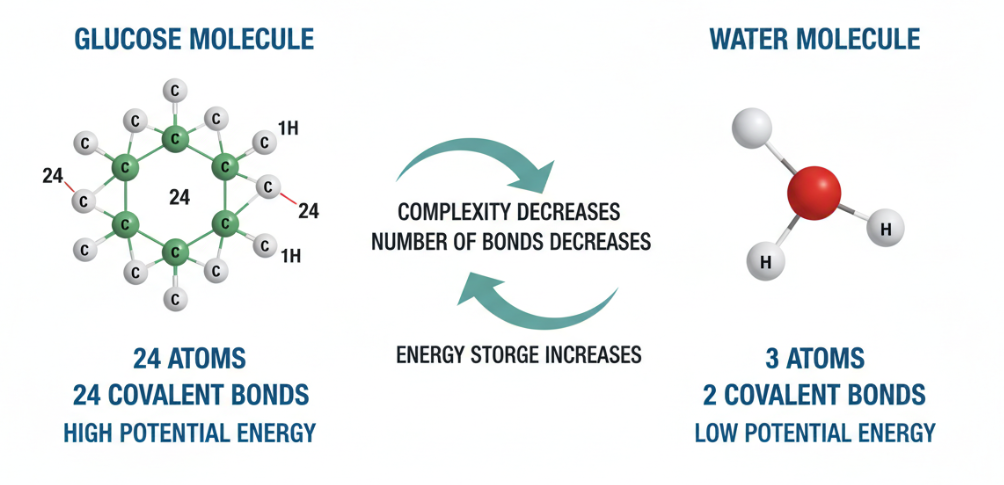
Art und Stabilität der chemischen Bindung
Der nächste Faktor ist der Schlüssel zum Verständnis des Energieunterschieds: die Art der chemischen Bindung und ihre Stabilität. Glukose enthält eine große Anzahl von Kohlenstoff-Kohlenstoff (C-C)- und Kohlenstoff-Wasserstoff (C-H)-Bindungen. Im Vergleich zu den sehr stabilen Sauerstoff-Wasserstoff-Bindungen (O-H) in Wasser sind diese C-C- und C-H-Bindungen relativ instabil und enthalten daher mehr Energie. Der Grund, warum der Energiezustand der O-H-Bindung von Wasser niedriger ist, liegt darin, dass das Sauerstoffatom eine hohe Elektronegativität aufweist, wodurch die Bindungselektronen stärker auf den Sauerstoff ausgerichtet sind und somit eine sehr stabile Struktur bilden. Dies erklärt, warum die Zellatmung ein energiefreisetzender Prozess ist. Bei diesem Prozess wird Glukose in Gegenwart von Sauerstoff in Kohlendioxid und Wasser zerlegt, beides energieärmere und stabilere Moleküle. Die bei diesem Prozess freigesetzte Energie ist im Wesentlichen das Ergebnis der Übertragung von Elektronen aus den hochenergetischen Zuständen der weniger elektronegativen Kohlenstoff- und Wasserstoffatome in der Glukose auf die elektronegativeren Sauerstoffatome, um einen energieärmeren, stabileren Zustand zu bilden.
An der Spitze der Ernährung
Wir bieten innovative Lösungen, die den Geschmack, die Beschaffenheit und das Nährwertprofil von Lebensmitteln verbessern, und unterstützen gesündere, nachhaltige Produkte für die Lebensmittelindustrie.
Oxidationszustand von Kohlenstoff
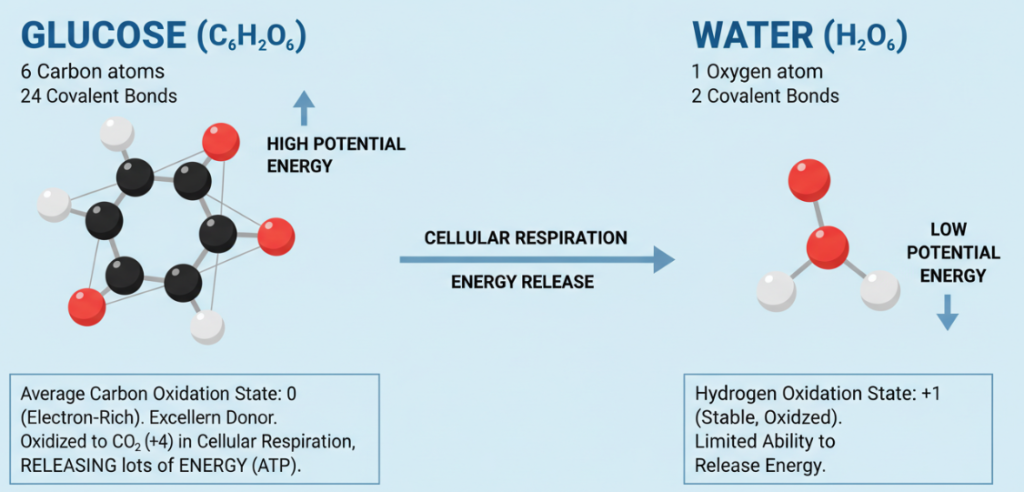
Schließlich ist noch der Oxidationszustand des Kohlenstoffatoms zu erwähnen, der als entscheidender Indikator für die hohe potenzielle Energie der Glukose angesehen werden kann. In Glukose befinden sich die Kohlenstoffatome in einem stark reduzierten Zustand, das heißt, sie sind elektronenreich. Nach der Berechnung ist die durchschnittliche Oxidationsstufe der Kohlenstoffatome in Glukose 0. Dieser Elektronenüberschuss macht Glukose zu einem hervorragenden Elektronendonator. Während der Zellatmung werden die Kohlenstoffatome der Glukose zu Kohlendioxid (CO₂) oxidiert. Im Kohlendioxid ändert sich die Oxidationsstufe des Kohlenstoffatoms auf +4, was bedeutet, dass es ein Elektron verloren hat. Die Elektronen bewegen sich zu den elektronegativeren Sauerstoffatomen und setzen dabei viel Energie frei, die dann in Form von ATP (3-Adenosinmonophosphat) für die Zellaktivität genutzt wird. Die Wasserstoffatome der Wassermoleküle hingegen befinden sich bereits in einem stabilen, oxidierten Zustand, und ihre Fähigkeit zur weiteren Energieabgabe ist sehr begrenzt.
Autor: Rechnung
Als leidenschaftlicher Spezialist mit einem tiefen Interesse an der Biochemie habe ich Jahre damit verbracht, komplexe wissenschaftliche Konzepte in klare, verständliche Inhalte zu zerlegen. In diesem Artikel befasse ich mich mit den molekularen Unterschieden, die Glukose im Vergleich zu Wasser zu einem Kraftpaket an potenzieller Energie machen. Ich hoffe, die grundlegenden Prinzipien zu beleuchten, die die Energie in biologischen Systemen bestimmen, und den Lesern dabei zu helfen, zu verstehen, warum diese beiden einfach erscheinenden Moleküle eine so unterschiedliche Rolle bei der Erhaltung des Lebens spielen.
 SGNUTRI
SGNUTRI