Qu'est-ce qui a le plus d'énergie potentielle : l'eau ou le glucose ?
L'énergie potentielle chimique stockée par les molécules de glucose (C≡H≡O₂) dépasse largement le niveau d'une molécule d'eau (H₂O). Cette différence significative peut être attribuée à trois facteurs fondamentaux au niveau moléculaire : la première est l'énorme différence de complexité moléculaire et le nombre de liaisons chimiques ; la deuxième est le type et la stabilité des liaisons chimiques ; et enfin, c'est l'état d'oxydation de l'atome de carbone. Ce sont ces facteurs qui déterminent que le glucose est la principale source d'énergie de la vie et que l'eau est le milieu stable de la réaction chimique de la vie.
Complexité moléculaire et nombre de liaisons chimiques
Tout d'abord, examinons la structure moléculaire. Une molécule de glucose est constituée de 24 atomes reliés par 24 liaisons covalentes, et sa structure est assez complexe. En revanche, une molécule d'eau n'est constituée que de trois atomes et de deux liaisons covalentes. Pour être honnête, il ne s'agit pas du tout d'une comparaison d'ordre de grandeur au niveau de la structure. L'énergie d'une molécule est stockée dans ses liaisons chimiques, de sorte que le plus grand nombre de liaisons chimiques dans le glucose lui permet de stocker beaucoup plus d'énergie potentielle que l'eau. Lorsque ces liaisons chimiques sont rompues au cours de processus tels que la respiration cellulaire, l'énergie stockée est libérée pour être utilisée par la cellule.
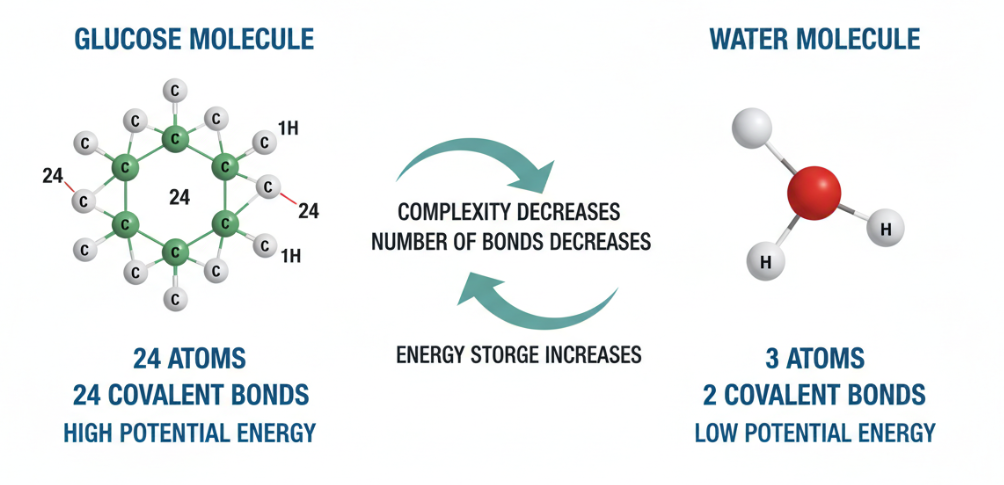
Type et stabilité des liaisons chimiques
Le facteur suivant est la clé pour comprendre la différence d'énergie : le type de liaison chimique et sa stabilité. Le glucose contient un grand nombre de liaisons carbone-carbone (C-C) et carbone-hydrogène (C-H). Comparées aux liaisons oxygène-hydrogène (O-H) très stables de l'eau, ces liaisons C-C et C-H sont relativement instables et contiennent donc une énergie plus élevée. La raison pour laquelle l'état énergétique de la liaison O-H de l'eau est plus faible est que l'atome d'oxygène a une forte électronégativité, ce qui fait que les électrons de liaison sont davantage orientés vers l'oxygène, formant ainsi une structure très stable. Cela explique pourquoi la respiration cellulaire est un processus qui libère de l'énergie. Dans ce processus, le glucose est décomposé en présence d'oxygène en dioxyde de carbone et en eau, deux molécules moins énergétiques et plus stables. L'énergie libérée par ce processus résulte essentiellement du transfert d'électrons des états de haute énergie des atomes de carbone et d'hydrogène les moins électronégatifs du glucose vers les atomes d'oxygène les plus électronégatifs pour former un état plus stable et de plus faible énergie.
À la pointe de la nutrition
Fournir des solutions innovantes qui améliorent la saveur, la texture et le profil nutritionnel des aliments, en soutenant des produits plus sains et durables pour l'industrie alimentaire.
État d'oxydation du carbone
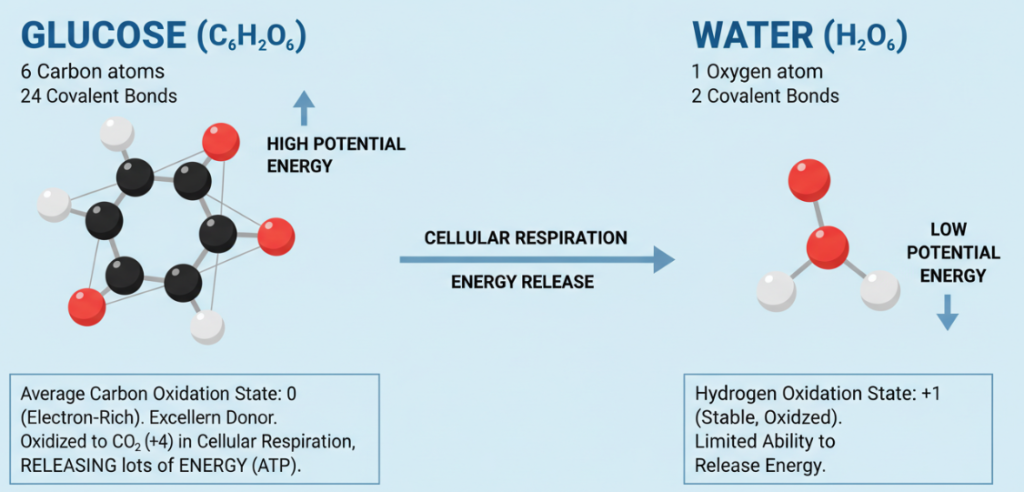
Enfin, il faut parler de l'état d'oxydation de l'atome de carbone, dont on peut dire qu'il est un indicateur décisif de l'énergie potentielle élevée du glucose. Dans le glucose, les atomes de carbone sont dans un état fortement réduit, c'est-à-dire qu'ils sont riches en électrons. Après calcul, l'état d'oxydation moyen des atomes de carbone du glucose est de 0. Ce surplus d'électrons fait du glucose un excellent donneur d'électrons. Au cours de la respiration cellulaire, les atomes de carbone du glucose sont oxydés pour former du dioxyde de carbone (CO₂). Dans le dioxyde de carbone, l'état d'oxydation de l'atome de carbone passe à +4, ce qui indique qu'il a perdu un électron. Les électrons se déplacent vers les atomes d'oxygène plus électronégatifs, libérant ainsi beaucoup d'énergie, qui est ensuite capturée sous forme d'ATP (3 adénosine monophosphate) pour alimenter l'activité cellulaire. En revanche, les atomes d'hydrogène des molécules d'eau sont déjà dans un état stable et oxydé, et leur capacité à libérer davantage d'énergie est très limitée.
Auteur : Projet de loi
En tant que spécialiste passionné par la biochimie, j'ai passé des années à transformer des concepts scientifiques complexes en un contenu clair et accessible. Dans cet article, je me penche sur les distinctions moléculaires qui font du glucose une centrale d'énergie potentielle par rapport à l'eau. J'espère éclairer les principes fondamentaux qui régissent l'énergie dans les systèmes biologiques et aider les lecteurs à comprendre pourquoi ces deux molécules d'apparence simple jouent des rôles si différents dans le maintien de la vie.
 SGNUTRI
SGNUTRI