Pourquoi le glucose est-il soluble dans l'eau ?
La principale raison pour laquelle le glucose se dissout dans l'eau est qu'il s'agit de deux "molécules polaires", ce qui permet aux molécules d'eau de former de fortes attractions appelées "liaisons hydrogène" avec les molécules de glucose. Plus précisément, une molécule de glucose possède plusieurs groupes hydroxyles (-OH) polaires. La molécule d'eau (H₂O) est également polaire, son atome d'oxygène étant légèrement négatif et ses atomes d'hydrogène légèrement positifs. Lorsque le glucose pénètre dans l'eau, les molécules d'eau, agissant comme de minuscules aimants, sont attirées par les groupes hydroxyles de la molécule de glucose et forment des liaisons hydrogène avec eux. Cette attraction est suffisamment puissante pour surmonter les forces qui maintiennent les molécules de glucose ensemble dans leur forme de cristal solide. Par conséquent, les molécules de glucose individuelles sont "arrachées" du cristal et se dispersent uniformément parmi les molécules d'eau, un processus que nous observons sous le nom de dissolution.
Polarité des molécules
En chimie, le principe de "ce qui se ressemble s'assemble" est fondamental et explique parfaitement la relation entre le glucose et l'eau. Tous deux font partie des molécules polaires, et c'est ce point commun qui détermine qu'ils peuvent "s'accepter" l'un l'autre. La polarité d'une molécule, pour dire les choses simplement, est l'uniformité de la distribution de ses charges internes. Celle-ci découle des différences d'"électronégativité", c'est-à-dire de la capacité des atomes à attirer les électrons partagés dans les liaisons chimiques.
Eau (H₂O) : Dans une molécule d'eau, les atomes d'oxygène sont beaucoup plus électronégatifs que les deux atomes d'hydrogène. Cela signifie que les électrons de liaison seront davantage orientés vers l'atome d'oxygène, lui conférant une faible charge négative (δ-), tandis que les deux atomes d'hydrogène se retrouveront avec une faible charge positive (δ+). Cette séparation des charges, associée au fait que la molécule d'eau elle-même est une structure "incurvée" en forme de V, en fait une molécule polaire très typique avec des extrémités positives et négatives claires.

Glucose (C₆H₁₂O₆) : Bien que la molécule de glucose soit beaucoup plus grosse, le principe est le même. Sa structure comporte de nombreux groupes hydroxyles (-OH). Dans chaque groupe hydroxyle, l'oxygène est plus électronégatif que l'hydrogène et le carbone qui lui sont attachés. Il en résulte une séparation importante des charges au sein de chaque groupe -OH, ce qui le rend très polaire. Avec autant de groupes hautement polaires sur une molécule, l'ensemble de la molécule de glucose devient naturellement une molécule polaire.
Liaisons hydrogène
C'est précisément parce que le glucose et l'eau sont polaires qu'ils créent les conditions nécessaires à la formation d'une force intermoléculaire puissante, la liaison hydrogène. Une liaison hydrogène est une attraction spéciale, assez forte. Elle se produit généralement entre un atome d'hydrogène lié à un atome fortement électronégatif (comme l'oxygène, l'azote ou le fluor) et un autre atome électronégatif proche.
Lorsque le glucose solide est placé dans l'eau, les molécules d'eau ont une extrémité hydrogène faiblement chargée positivement et sont fortement attirées par les atomes d'oxygène faiblement chargés négativement dans le groupe hydroxyle du glucose. Inversement, l'extrémité oxygène faiblement chargée négativement de la molécule d'eau est également attirée par les atomes d'hydrogène faiblement chargés positivement du groupe hydroxyle du glucose. Ce réseau d'attraction entre ces deux molécules constitue l'essence de la liaison hydrogène dans ce scénario.
À la pointe de la nutrition
Fournir des solutions innovantes qui améliorent la saveur, la texture et le profil nutritionnel des aliments, en soutenant des produits plus sains et durables pour l'industrie alimentaire.
Processus de dissolution
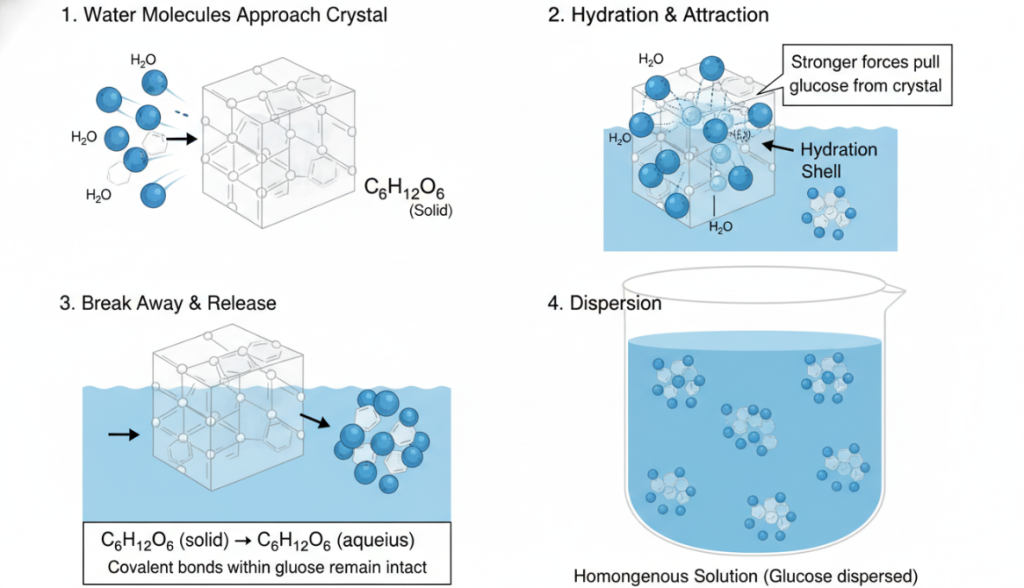
La dissolution du glucose est un processus dynamique au niveau moléculaire.
Les molécules d'eau s'approchent des cristaux : À l'état solide, le glucose existe sous la forme d'un réseau cristallin, et les molécules individuelles sont maintenues les unes aux autres par leurs propres forces intermoléculaires. Lorsque ce cristal est jeté dans l'eau, les molécules d'eau en mouvement commencent à frapper sa surface.
Hydratation et attraction : Les molécules d'eau polaires entourent immédiatement les molécules de glucose à la surface du cristal. En formant un grand nombre de liaisons hydrogène, l'attraction d'un groupe de molécules d'eau sur une seule molécule de glucose devient plus forte que la force entre cette molécule de glucose et ses voisines dans le cristal.
Se détache et se libère : Cette puissante "traction" exercée par les molécules d'eau tire effectivement les molécules de glucose individuelles hors de la structure solide. Il faut souligner ici que la molécule d'eau ne rompt pas les liaisons covalentes fortes au sein de la molécule de glucose ; elle ne rompt que les forces intermoléculaires plus faibles qui maintiennent la structure cristalline. Il en résulte que les molécules de glucose intactes se détachent du cristal et passent en solution. Ce processus est généralement exprimé par l'équation suivante : C₆H₁₂O₆ (solide) → C₆H₁₂O₆ (aqueux).
Auteur:Derek
Ma passion est de démystifier la chimie. J'aime prendre une question simple, comme "pourquoi le sucre se dissout-il dans l'eau ?", et révéler l'élégante science moléculaire qui la sous-tend, en me concentrant sur des idées fondamentales telles que la polarité et le pouvoir de la liaison hydrogène.
 SGNUTRI
SGNUTRI